Amoniac còn gọi là NH3, một trong những hoá chất có rất nhiều trong tự nhiên, được ứng dụng rộng rãi trong sản xuất công nghiệp. Để hiểu rõ hơn về amoniac là gì, tính chất, ứng dụng, cách điều chế, tác hại,… của loại chất này sẽ được chúng tôi thông tin đầy đủ, chi tiết ngay sau đây!
Tóm tắt
Thông tin cơ bản về Amoniac
Amoniac (NH3) là gì?
Amoniac là hợp chất của Nitơ (N) và Hydro (H) với công thức hoá học là NH3. Đây là một hợp chất vô cơ được cấu tạo bởi 3 nguyên tử Nitơ, 1 nguyên tử Hydro giúp tạo nên thành 1 liên kết kém bền.
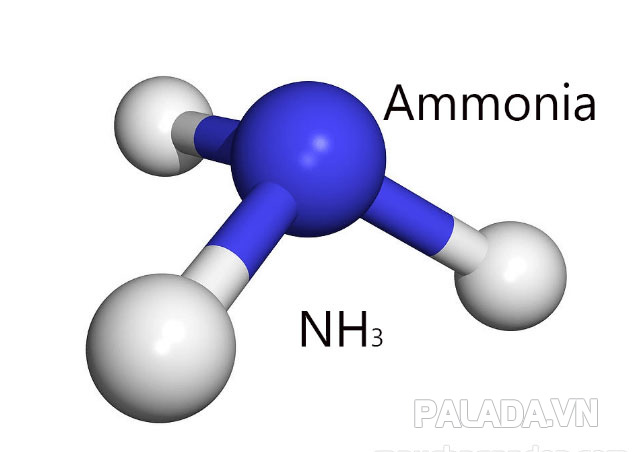
Cấu tạo phân tử của NH3 là hình chóp, có nguyên tử nitơ ở đỉnh liên kết cộng hóa trị với 3 nguyên tử Hidro ở đáy tam giác. Nh3 sinh ra nhiều ở trong tự nhiên, trong đó thận của chúng con người cũng sản sinh ra một lượng nhỏ khí NH3, cho nên nước tiểu có mùi khai đặc trưng tương tự như khí amoniac.
Mùi của Amoniac
Amoniac có mùi hăng, khai đặc trưng, có thể nhận biết mùi của Amoniac trong thành phần của nước tiểu động vật, vì trong quá trình chuyển hóa thức ăn cơ thể con người đã bài tiết ra một lượng Nitơ khi kết hợp với các chất hữu cơ khác giúp sinh ra khí NH3.
Nếu như không may hít phải khí NH3 với nồng độ lớn có thể dẫn tới tử vong, bởi vì khi NH3 vào niêm mạc mũi và phổi với nồng độ cao sẽ phản ứng với H2O trong cơ thể, làm sinh ra NH4OH có tính bazơ có khả năng ăn mòn cao, làm phá huỷ nội tạng của con người. Đây là hợp chất hoá học đặc biệt nguy hiểm, cho nên cần phải đặc biệt thận trọng khi sử dụng.
Amoniac có ở đâu?
Amoniac có rất nhiều xung quanh chúng ta như:
- Khí nh3 hình thành bởi các sinh vật trong tự nhiên từ quá trình phân hủy của xác động vật bởi tác động của các vi sinh vật và được tìm thấy với lượng nhỏ trong khí quyển.
- Amoniac còn có ở một số muối amoni trong nước biển.
- Muối amoni clorua, amoni sunfat được sản sinh ra từ các vụ phun trào núi lửa.
- Các tinh thể amoni bicacbonat có trong 1 số khoáng chất chứa soda.

Tính chất của NH3
Tính chất vật lý
NH3 có đặc điểm vật lý như sau:
- Amoniac thường ở thể khí, không màu, có mùi khó chịu. Với nồng độ amoniac cao có thể gây ra tử vong.
- Amoniac rất phân cực, bởi phân tử NH3 có một cặp electron độc thân và liên kết N-H phân cực. Vì thế, NH3 có thể hóa lỏng dễ dàng.
- Dung dịch amoniac là dung môi tốt, có thể hòa tan các dung môi hữu cơ dễ hơn nước bởi hằng số điện môi của chúng thấp hơn nước. Kim loại kiềm và kim loại Ca, Sr, Ba có thể tan được trong NH lỏng, giúp tạo ra dung dịch màu xanh thẫm.
Tính chất hóa học
Đặc điểm tính chất hoá học của amoniac như sau:
- Khi NH3 hòa tan trong nước sẽ có một phần nhỏ phân tử amoni được kết hợp với ion H trong nước giúp tạo thành cation amoni, giải phóng anion. Lúc này nước đóng vai trò là axit.
- Dung dịch amoniac làm quỳ tím chuyển sang màu xanh và làm cho dung dịch phenolphtalein chuyển sang màu hồng bởi tính kiềm. Để phát hiện amoniac sẽ sử dụng quỳ tím ướt.
- Amoniac có thể dễ bị phân hủy trong dung dịch, làm giải phóng khí amoniac.
- Khi phản ứng với axit, Amoniac lỏng trung hòa axit, tạo thành muối amoni.
- Khi phản ứng với dung dịch muối, amoni có khả năng tạo thành nhiều hiđroxit kim loại ở thể khí dễ phản ứng.
- Amoniac là chất khử
- NH3 kém bền dưới tác động của nhiệt, chúng có thể bị phân hủy ở nhiệt độ cao bởi phản ứng hóa học: 2NH3 → N2 + 3H2 N2 + 3H2 → 2NH3
- Tác dụng với ion kim loại chuyển tiếp tạo ion phức: 2NH3 + Ag+ → [Ag(NH3)2]+
- Nguyên tử hiđro của amoniac có thể thay thế bằng kim loại kiềm hay nguyên tử nhôm:
2NH3 + 2Na → 2NaNH2 + H2 (350 °C)
2NH3 + 2Al → 2AlN + 3H2 (800-900 °C)
Đặc điểm tính chất hoá học của amoniac
Ứng dụng của Amoniac ở trong đời sống
Có thể thấy NH3 vô cùng phổ biến trong tự nhiên, được ứng dụng rộng rãi trong đời sống và sản xuất như:
- NH3 hoá lỏng được dùng trong quá tình lý khí thải của các nhà máy luyện gang thép, xi măng, nhiệt điện, lọc hóa dầu,… giúp không gây ô nhiễm môi trường.
- NH3 được dùng trong sản xuất phân bón bởi các hợp chất N trong phân đạm rất cần thiết cho sự phát triển của cây trồng, giúp cung cấp năng suất của các loại cây trồng như ngô, lúa mì.
- Dung dịch NH3 còn được dùng để làm thuốc tẩy cho nhiều bề mặt như: thủy tinh, đồ sứ, thép không gỉ, ngoài ra còn được dùng để làm sạch lò nướng, ngâm đồ giúp làm sạch bụi bẩn.
- NH3 còn dùng để giúp làm tối màu gỗ, Amoniac phản ứng với tanin tự nhiên trong gỗ làm thay đổi màu gỗ trở nên đẹp hơn.
- Trong công nghiệp thực phẩm, dung dịch amoniac dùng để điều chỉnh độ chua. Amoniac lỏng dùng với mục đích thương mại giúp loại bỏ nhiễm khuẩn của thịt bò.
- Ứng dụng trong ngành công nghiệp khai thác mỏ, dùng để khai thác các kim loại như đồng Ni (niken) và Mo (molypden)
- Trong ngành dầu khí Nh3 có tác dụng giúp trung hòa axit, bảo vệ các thiết bị khỏi bị ăn mòn.
Cách để điều chế Amoniac
Amoniac trong phòng thí nghiệm
Người ta dùng muối NH4Cl tác dụng với nước vôi trong Ca(OH)2 giúp sinh ra khí NH3 như phương trình phản ứng sau đây:
2NH4Cl + Ca(OH)2 → NH3 (khí) + CaCl2 + H2 (khí)
Amoniac trong công nghiệp
Nh3 chủ yếu được sản xuất theo phương thức Haber-Bosch với những phản ứng 2 chiều được xảy ra liên tiếp sau:
CH4 + H2O < == > CO + 3H2 (xúc tác Ni, nhiệt độ cao)
N2 + 3H2 < == > 2NH3 (ΔH = –92 kJ/mol)
Amoniac được điều chế trong công nghiệp
Để điều chế NH3 trong công nghiệp, người ta thường dùng công nghệ sản xuất amoniac như:
- Công nghệ Haldor Topsoe
- Công nghệ M.W. Kellogg
- Công nghệ Krupp Uhde
- Công nghệ ICI
- Công nghệ Brown & Root
Trong đó công nghệ Haldor Topsoe được áp dụng tại các nhà máy phân đạm tại Việt Nam nhằm để sản xuất NH3.
Do vừa có tính ăn mòn, lại nguy hiểm, vì thế việc sản xuất, lưu trữ phải được tuân thủ theo quy trình nghiêm ngặt. Trong công nghiệp NH3 nám dưới dạng khí hóa lỏng và dung dịch amoniac NH4OH. Tất cả đều được vận chuyển trong xe bồn hay ống trụ.
Xem thêm: Phản ứng phân hủy là gì? Đặc tính, ví dụ về phản ứng phân hủy
Tác hại của Amoniac, cách xử lý khi ngộ độc amoniac
Tác hại của amoniac
Thường thì chỉ cần hít phải lượng nhỏ NH3 cũng khiến cho chúng ta cảm thấy khó chịu. Nhưng trên thực tế thì NH3 còn được xếp vào chất nguy hiểm và đặc biệt nguy hiểm với sức khỏe của con người bởi:
- Nếu như hít phải: Sẽ gây bỏng niêm mạc mũi, cổ họng và đường hô hấp. Từ đó, làm phá hủy đường thở dẫn tới tình trạng bị suy hô hấp, bởi vì amoniac có tính ăn mòn.
- Tiếp xúc trực tiếp: với da, mắt, họng, phổi sẽ gây ra vấn đề bị bỏng nặng. vết bỏng có thể gây mù vĩnh viễn, bệnh phổi thậm chí là tử vong.
- Nuốt phải: Nếu như nuốt phải amoniac đậm đặc sẽ gây bỏng ở miệng, cổ họng và dạ dày, dẫn tới đau dạ dày nghiêm trọng, gây nôn.
NH3 cực nguy hiểm đối với sức khoẻ của con người
Xử lý khi ngộ độc amoniac
Amoniac nồng độ cao đặc biệt độc với con người, nhưng không phải ai cũng biết cách để xử lý nếu như không may tiếp xúc và bị ngộ độc khí amoniac. Sau đây là một số cách giúp sơ cứu khi bị ngộ độc amoniac bạn nên biết:
- Nếu như hít phải khí amoniac, cần nhanh chóng di chuyển nạn nhân đến nơi thoáng khí và cởi sạch quần áo bị dính amoniac.
- Súc sạch miệng nếu như nuốt phải amoniac. Sau đó cho nạn nhân uống từ 1-2 cốc sữa.
- Nếu như da tiếp xúc với amoniac nên chú ý rửa sạch amoniac dính trên da bằng xà phòng và nước. Rửa lại sạch mắt với thật nhiều nước.
- Đưa nạn đến trạm y tế và bệnh viện gần nhất để xử lý.
Hướng dẫn bảo quản, vận chuyển NH3 an toàn
Cách bảo quản
- Nên thực hiện bảo quản NH3 trong các bồn lỏng hay bình chứa có ghi nhãn mác rõ ràng.
- Chú ý không nên nạp NH3 lỏng đầy quá 80% thể tích của thiết bị chứa
- Lưu trữ NH3 ở trong thùng kín tại những nơi khô ráo, thoáng mát, riêng biệt, đảm bảo thông gió tốt.
- Tránh xa chất này khỏi những nơi có thể gây cháy.
- Tránh nhiệt, độ ẩm và những vật tương khắc.
Hướng dẫn bảo quản NH3 tốt nhất
Cách vận chuyển
- Với NH3 công nghiệp được bán dưới dạng dung dịch amoniac hay amoniac lỏng nên chứa trong bồn lỏng để vận chuyển bằng xe ô tô hay bình chứa.
- Phương tiện vận chuyển yêu cầu cần phải có mái che, thành xe chắc chắn.
- Không chở lẫn người cùng những vật liệu dễ cháy, bình được xếp ở tư thế đứng một lượt. Lưu ý ở giữa của các bình phải có đệm lót, bốc xếp nhẹ nhàng, tránh để sản phẩm ở những nơi có nhiệt độ cao.
Bài viết trên đây của chúng tôi đã giúp bạn đọc trả lời được cho câu hỏi amoniac là gì, cũng như những điều quan trọng cần biết về hợp chất này. Đửng quên theo dõi palada.vn để cập nhật thêm cho mình nhiều thông tin hữu ích nhé!

